Avertissement : Cette page est destinée uniquement aux professionnels de la santé.
À propos de WelivaMD CimidonaMD
WelivaMD CimidonaMD est un produit en vente libre, disponible sans ordonnance. Cette solution sans hormones destinée aux femmes adultes à n’importe quel stade de la ménopause contient un ingrédient actif de source naturelle qui aide à réduire la fréquence et la sévérité des symptômes de la ménopause1.
Autres points importants concernant WelivaMD CimidonaMD qui peuvent vous aider à orienter votre recommandation :
Indiqué pour les femmes adultes à n’importe quel stade de la ménopause1 pour aider à soulager efficacement les multiples symptômes liés à la ménopause1
Contient Ze 450, un extrait exclusif d’Actaea racemosa
Aide à réduire la fréquence et la sévérité des symptômes de la ménopause, notamment les bouffées de chaleur, les sueurs nocturnes, la fatigue, l’irritabilité, la nervosité, l’insomnie, les douleurs articulaires légères, les troubles de la concentration, les palpitations et les maux de tête1,2
Offert en comprimés de 13 mg1
La posologie recommandée est d’un comprimé par jour1
Les patientes peuvent s’attendre à ressentir les effets de WelivaMD CimidonaMD après au moins 6 semaines d’utilisation1
*Natural Product Number (NPN) 80125992.1
Comprendre l’extrait Ze 450
L’Actaea racemosa (également connue sous le nom d’actée à grappes noires)1 est une plante médicinale vivace traditionnellement utilisée pour traiter divers troubles, notamment les symptômes liés à la ménopause2.
Bien que le mécanisme d’action de l’Actaea racemosa n’ait pas encore été entièrement élucidé, des données indiquent que Ze 450 agit par le biais de voies neurohormonales non œstrogéniques. Des études expérimentales montrent une activité agoniste partielle au niveau des récepteurs de la sérotonine (5-HT1A, 5-HT1D, 5-HT7) et des récepteurs opiacés µ, lesquels contribuent à la thermorégulation hypothalamique. En modulant ces récepteurs, Ze 450 pourrait stabiliser le centre de contrôle de la température dans le cerveau et ainsi réduire la fréquence et l’intensité des bouffées de chaleur2-7.
Puisque des études in vitro ont démontré que Ze 450 n'a aucun effet œstrogénique, il pourrait être considéré comme une alternative non hormonale au traitement hormonal de la ménopause (THM)4,5.

WelivaMD CimidonaMD Ze 450 a fait l’objet de plusieurs études cliniques
L’efficacité et l’innocuité de Ze 450 ont été cliniquement démontrées dans le cadre d’un essai randomisé contrôlé par placebo, d’un essai prospectif ouvert et d’une étude observationnelle rétrospective.
Aperçu des études :
| ÉTUDES | CONCEPTION | TRAITEMENT‡ | PRINCIPAL RÉSULTAT ANALYSÉ |
|---|---|---|---|
| Schellenberg 20122 | Étude multicentrique randomisée, en double aveugle, contrôlée par placebo, d’une durée de 12 semaines, avec groupes parallèles*
n=180 |
CimidonaMD Ze 450 13 mg Placebo | Critère d’évaluation principal : différence au niveau de la sévérité des symptômes de la ménopause, tels qu’évalués à l’aide du score total KMI (indice ménopausique de Kupperman) modifié, entre le début de l’étude et la semaine 12. |
| Drewe 20138 | Étude prospective observationnelle ouverte, multicentrique, d’une durée de 12 semaines, avec prolongation additionnelle de 6 mois†
n=422 |
CimidonaMD Ze 450 13 mg | Critère d’évaluation principal : différence au niveau de la sévérité des symptômes de la ménopause, tels qu’évalués à l’aide du score total KMI modifié, entre le début de l’étude et la semaine 12. |
| Friederichsen 20203 | Étude de cohorte rétrospective monocentrique observationnelle†
n=174 |
CimidonaMD Ze 450 13 mg ou traitement hormonal de la ménopause (THM) | Paramètres métaboliques sériques, poids corporel et symptômes ménopausiques évalués à l’aide de l’échelle d’évaluation de la ménopause (MRS-II) |
*Schellenberg (2012) : Les groupes de traitement étaient Ze 450 6,5 mg (n = 57), Ze 450 13 mg (n = 55) et placebo (n = 54). La comparaison principale a été effectuée entre le groupe recevant 13 mg et le groupe recevant le placebo (totalisant 109 participantes). Le critère d’évaluation principal était l’évolution des symptômes de la ménopause selon l’indice ménopausique de Kupperman2
†Drewe (2013) : Ze 450 à des doses de 1 x 6,5 mg ou 2 x 13 mg d’extrait sec a également été utilisé. Dans l'étude de Friederichsen (2019), Ze 450 à des doses de 1 x 6,5 mg a également été utilisé3,8
†‡Seul WelivaMD CimidonaMD 13 mg est approuvé pour utilisation au Canada1.
Étude Schellenberg (2012)2*
Aperçu de l’étude :
Schellenberg a étudié 180 femmes âgées de plus de 40 ans souffrant de troubles ménopausiques pendant 12 semaines2. Cette étude multicentrique randomisée, en double aveugle, contrôlée par placebo, avec groupes parallèles, d’une durée de 12 semaines (n = 109) a évalué l’efficacité de l’extrait Ze 450 d’Actaea racemosa, 13 mg, n = 55†‡) par rapport à un placebo (n = 54). Le critère d’évaluation principal était la différence dans la sévérité des symptômes de la ménopause, mesurée à l’aide d’un score total modifié (KMI) entre la semaine 12 et le début de l’étude2.
CimidonaMD Ze 450 13 mg a significativement atténué les symptômes de la ménopause§
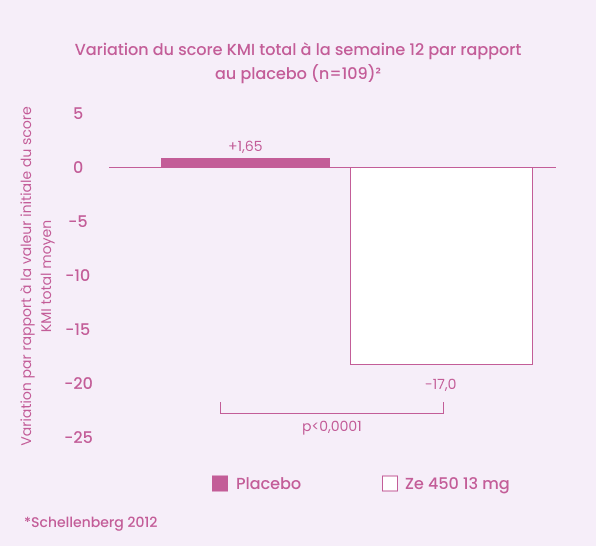
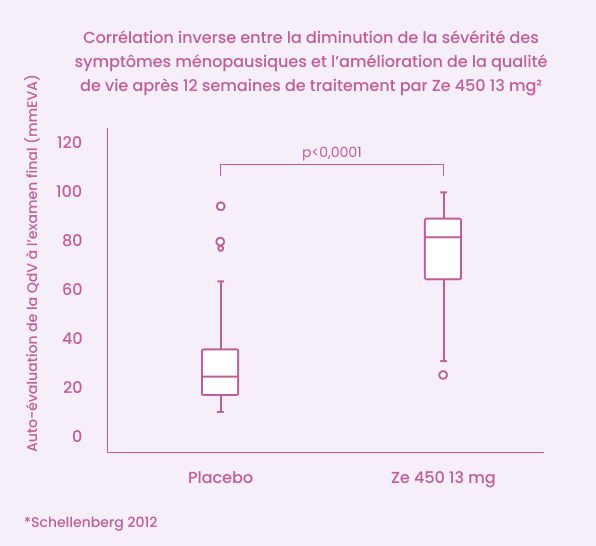
L’extrait Ze 450 s’est révélé supérieur au placebo dans la réduction de la sévérité globale des symptômes de la ménopause (vasomoteurs, psychologiques et somatiques)2
Points clés:
Réduction significative de la sévérité des symptômes de la ménopause (vasomoteurs, psychologiques et somatiques) par rapport au placebo2
Amélioration significative de la qualité de vie (QdV) auto-évaluée2¶
Ze 450 s’est révélé être une option thérapeutique non hormonale efficace et bien tolérée pour soulager les symptômes de la ménopause2
Disponible uniquement en anglais
*Étude randomisée, en double aveugle, contrôlée par placebo – par rapport au placebo (p < 0,0001) Les patientes ont pris quotidiennement l’extrait Ze 450 (13 mg) ou un placebo pendant une période de 12 semaines. Le critère d’évaluation principal était la différence entre les symptômes ménopausiques ressentis (vasomoteurs, psychologiques et somatiques) observés entre la semaine 12 et la valeur de référence établie2.
†Schellenberg (2012) : Ze 450 à une dose de 6,5 mg d’extrait sec faisait également partie du groupe de traitement (n = 57)2.
‡Seul WelivaMD CimidonaMD 13 mg est approuvé pour utilisation au Canada1.
§Les données sont présentées pour les personnes ayant reçu uniquement Ze 450 13 mg. Seul WelivaMD CimidonaMD 13 mg est approuvé pour utilisation au Canada.1
¶ Évalué à l’aide d’une échelle visuelle analogique de 100 mm2.
Étude Drewe (2013)8*
Aperçu de l’étude :
Drewe a observé 442 femmes souffrant de troubles ménopausiques pendant 12 semaines8. Cette étude prospective observationnelle ouverte, multicentrique, d’une durée de 12 semaines, prolongée de 6 mois (n = 228), a évalué l’extrait Ze 450 d’Actea racemosa, 13 mg†‡ ). Le critère d’évaluation principal était la variation de la sévérité des symptômes de la ménopause, mesurée à l’aide d’un score total modifié (KMI) entre la semaine 12 et le début de l’étude8.
Soulagement à long terme des symptômes de la ménopause avec CimidonaMD Ze 450.
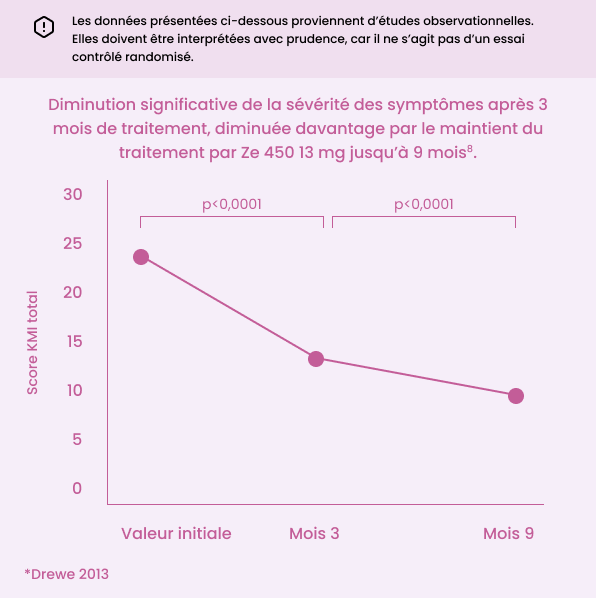
Points clés :
Réduction significative de la sévérité des symptômes de la ménopause après 3 mois de traitement8
Le maintient du traitement a amélioré les symptômes de la ménopause avec un soulagement significatif après 9 mois8
Ze 450 a été très bien toléré8
*Étude observationnelle - (p < 0,001) Les patientes ont pris 1 comprimé de CimidonaMD 13 mg par jour pendant une période de 3 mois. Au cours de la prolongation de 6 mois qui a suivi, certain patientes sont passées à une dose de 6,5 mg (n = 102), tandis que d’autres ont continué à prendre la dose de 13 mg (n = 228). Les résultats ont mesuré les scores totaux de sévérité de la ménopause et ses sous-items après 3 mois et après 9 mois par rapport à la valeur initiale8.
†Drewe (2013): Ze 450 à des doses de 1 x 6,5 mg (n = 27 en phase 1, n = 131 en phase 2) ou 2 x 13 mg (n = 23 en phase 1, n = 12 en phase 2) d’extrait sec a également été utilisé8.
‡Seul WelivaMD CimidonaMD 13 mg est approuvé pour utilisation au Canada1.
Étude Friederichsen (2019)3*
Aperçu de l’étude :
Friederichsen a étudié rétrospectivement 174 femmes âgées de plus de 40 ans présentant des symptômes de la ménopause3. Cette étude de cohorte observationnelle monocentrique a comparé l’extrait de Ze 450 d’Actaea racemosa (Ze 450, 1x13 mg [n=25] ou 1x6,5 mg [n=7]†‡) à un traitement hormonal de la ménopause (THM) (n=142). Les résultats comprenaient les paramètres métaboliques sériques, le poids corporel et les symptômes de la ménopause évalués à l’aide de l’échelle d’évaluation de la ménopause3.
Ze 450 13 mg a atténué la sévérité des symptômes de la ménopause sans différence notable par rapport à un THM.
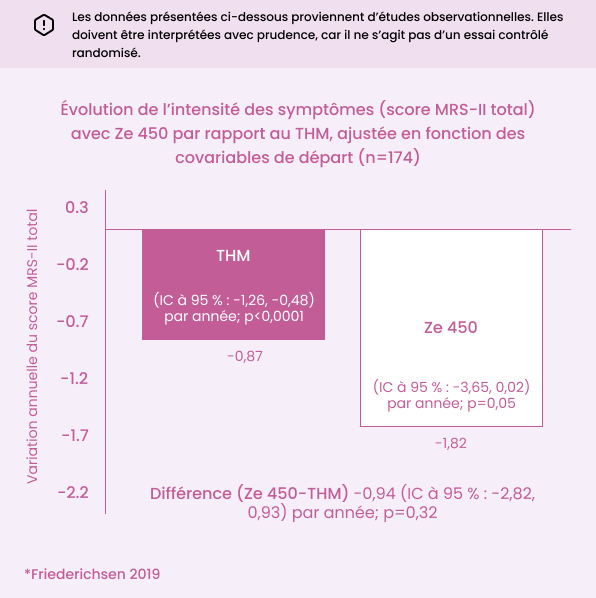
L’extrait Ze 450 et le THM ont tous deux réduit la sévérité des symptômes de la ménopause sans différence notable entre les deux groupes3.
Points clés :
Améliorations significatives au niveau des symptômes de la ménopause dans les deux groupes3
Aucune variation du poids corporel n’a été observée au cours de la période d’étude dans les deux groupes3
Disponible uniquement en anglais
*Étude de cohorte rétrospective monocentrique : des femmes présentant des symptômes ménopausiques qui avaient eu leur première consultation entre 2009 et 2016 ont été sélectionnées. Les participantes admissibles étaient celles traitées soit par THM, soit par l’extrait Ze 450 d’Actaea racemosa (CimidonaMD) et qui avaient eu au moins une consultation de suivi au cours de la période d’observation de 12 mois. Les groupes de traitement comprenaient Ze 450 à 6,5 mg (n = 7) ou 13 mg (n = 25) et un THM (n = 142). Les résultats ont été évalués rétrospectivement, en se concentrant sur les comparaisons entre Ze 450 (les deux doses combinées) et le THM en ce qui concerne les paramètres métaboliques et le poids corporel. Les critères d’évaluation principaux comprenaient les paramètres métaboliques sériques (lipides, glucose, insuline et HOMA-IR), le poids corporel et les symptômes de la ménopause évalués à l’aide de l’échelle d’évaluation de la ménopause (MRS-II). L’analyse statistique a utilisé des modèles de régression linéaire à effets mixtes univariables et multivariables supposant un effet linéaire du temps3.
†Seul WelivaMD CimidonaMD 13 mg est approuvé au Canada. Dans cette étude, pour la dose de 13 mg, CimifeminMD forte et ClimavitaMD Forte ont été utilisés. Il s’agit de marques européennes équivalentes à CimidonaMD au Canada3.
WelivaMD CimidonaMD Ze 450 13 mg a été généralement bien toléré2,8
Les essais cliniques confirment le profil d'innocuité positif de WelivaMD CimidonaMD pour une durée de traitement pouvant aller jusqu'à 9 mois2,8. Les effets indésirables liés au traitement étaient rares et sans gravité. Les plaintes les plus courantes étaient de nature gastro-intestinale (p. ex. les nausées et douleurs abdominales2,8.
Conseiller vos patientes sur la prise de WelivaMD CimidonaMD
Recommandez à vos patientes de prendre 1 comprimé par jour1, et d’utiliser le produit pendant au moins 6 semaines pour constater des effets bénéfiques1.
Recommandez à vos patientes de vous consulter ou de consulter leur pharmacien si leurs symptômes persistent ou s’aggravent, ou si elles souffrent d’une affection hépatique ou développent des symptômes de troubles hépatiques.
Ne recommandez pas ce produit à vos patientes enceintes ou qui allaitent1.
Références :
- Santé Canada. Licence de produit WelivaMD CimidonaMD. Émise le 4 août 2023.
- Schellenberg R, Saller R, Hess L, et al. Dose-Dependent Effects of the Cimicifuga racemosa Extract Ze 450 in the Treatment of Climacteric Complaints: A Randomized, Placebo-Controlled Study. Evid Based Complement Alternat Med. 2012;2012:260301. doi:10.1155/2012/260301. [Disponible uniquement en anglais]
- Friederichsen L, Nebel S, Zahner C, Bütikofer L, Stute P. Effect of CIMicifuga racemosa on metaBOLIC parameters in women with menopausal symptoms: a retrospective observational studystudy (CIMBOLIC). Arch Gynecol Obstet. 2020;301(2):517-523. doi:10.1007/s00404-019-05366-8. [Disponible uniquement en anglais]
- Garita-Hernandez M, Calzado MA, Caballero FJ, et al. The growth inhibitory activity of the Cimicifuga racemosa extract Ze 450 is mediated through estrogen and progesterone receptors-independent pathways. Planta Med. 2006;72(4):317-323. doi:10.1055/s-2005-916233. [Disponible uniquement en anglais]
- Wuttke W, Seidlová-Wuttke D. Black cohosh (Cimicifuga racemosa) is a non-estrogenic alternative to hormone replacement therapy. Clinical Phytoscience. 2015;1(1):12. doi:10.1186/s40816-015-0013-0
- Drewe J, Bucher KA, Zahner C. A systematic review of non-hormonal treatments of vasomotor symptoms in climacteric and cancer patients. Springerplus. 2015;4:65. Publié le 10 février 2015. doi:10.1186/s40064-015-0808-y. [Disponible uniquement en anglais]
- Rhyu MR, Lu J, Webster DE, Fabricant DS, Farnsworth NR, Wang ZJ. Black cohosh (Actaea racemosa, Cimicifuga racemosa) behaves as a mixed competitive ligand and partial agonist at the human mu opiate receptor. J Agric Food Chem. 2006;54(26):9852-9857. doi:10.1021/jf062808u.
- Drewe J, Zimmermann C, Zahner C. The effect of a Cimicifuga racemosa extracts Ze 450 in the treatment of climacteric complaints--an observational study. Phytomedicine. 2013;20(8-9):659-666. doi:10.1016/j.phymed.2013.02.012. [Disponible uniquement en anglais]
Avertissements :
- Toujours diriger la patiente à lire l’étiquette. Pour plus d’informations, veuillez consulter les Mises en garde, Précautions et Mode d’emploi disponibles à l’adresse suivante : https://health-products.canada.ca/lnhpd- bdpsnh/info?licence=80034529&lang=fre afin d’aider à l’évaluation bénéfice risque. Les conditions de l’Autorisation de mise en marché sont également disponibles sur demande en nous appelant au 1 888 550 6060.
Avis de non-responsabilité : cette page est destinée uniquement aux professionnels de la santé.
You will be redirected to the Pharmilink website
Enter your details to receive a product sample from Weliva

Thank you!
For confirming your interest in Weliva and your commitment to improving menopausal health. You will receive an email confirmation from us shortly.


